Keshe Foundation - Betrug und kein Ende in Sicht?
16.614 Beiträge ▪ Schlüsselwörter:
Iran, Freie Energie, Weltfrieden ▪ Abonnieren: Feed E-Mail
Keshe Foundation - Betrug und kein Ende in Sicht?
24.03.2014 um 20:29@Konfuse:
Es gibt auch noch eine andere Variante des Experiments (nach den Aussagen im letzten Workshop scheint das Keshe's eigener Aufbau zu sein), bei der statt der Kupfer-Elektrode ein silberfarbenes Metallblech (Zink wäre naheliegend) verwendet wird. Mit dieser Variante lässt sich ein Lüfter betreiben, wie im Video zu sehen ist. Das ist aber offensichtlich nichts anderes als eine primitive Batterie. Ich würde die Leistung pro Zelle da mal sehr grob auf ein oder vielleicht ein paar Milliwatt schätzen, also etwa das tausendfache von dem, was die Kupfer/Kupferoxid-Zellen liefern können. Einige dutzend Zellen reichen da für einen Low-Power-Lüfter. Amüsanterweise schreiben die Knowledge Seeker im Workshop den Umstand, dass der Lüfter bei Keshe's Aufbau läuft, und bei ihrem nicht, Keshe's grösserer Erfahrung zu. ;)
Es sieht vielleicht etwas verwirrend aus, aber die Zellen sind in Reihe geschaltet. Das ist soweit schon in Ordnung. Bei der Kupfer/Kupferoxid-Variante des Experiments, auf die ich oben verlinkt hatte, dürfte die Leistung pro Zelle allerdings im sehr niedrigen Mikrowatt-Bereich liegen. Da reichen auch 50 Zellen nicht für einen Lüfter.Konfuse schrieb:Die schließen die Elektroden ja kurz, wie soll da eine Potentialdifferenz entstehen.
Es gibt auch noch eine andere Variante des Experiments (nach den Aussagen im letzten Workshop scheint das Keshe's eigener Aufbau zu sein), bei der statt der Kupfer-Elektrode ein silberfarbenes Metallblech (Zink wäre naheliegend) verwendet wird. Mit dieser Variante lässt sich ein Lüfter betreiben, wie im Video zu sehen ist. Das ist aber offensichtlich nichts anderes als eine primitive Batterie. Ich würde die Leistung pro Zelle da mal sehr grob auf ein oder vielleicht ein paar Milliwatt schätzen, also etwa das tausendfache von dem, was die Kupfer/Kupferoxid-Zellen liefern können. Einige dutzend Zellen reichen da für einen Low-Power-Lüfter. Amüsanterweise schreiben die Knowledge Seeker im Workshop den Umstand, dass der Lüfter bei Keshe's Aufbau läuft, und bei ihrem nicht, Keshe's grösserer Erfahrung zu. ;)
Keshe Foundation - Betrug und kein Ende in Sicht?
24.03.2014 um 21:25Stimmt, habe ich komischerweise gar nicht dran gedacht. Aber 50 Zellen in Reihe und so ein simpler Lüfter läuft nicht, ist natürlich kein Erfolgserlebnis. Dummerweise ist die CuO-Schicht auch noch ein schlechter Leiter, was die Sache natürlich nicht effektiver macht.uatu schrieb:Es sieht vielleicht etwas verwirrend aus, aber die Zellen sind in Reihe geschaltet. Das ist soweit schon in Ordnung.
Ja, der größeren Erfahrung im Trikxen ;)uatu schrieb:Amüsanterweise schreiben die Knowledge Seeker im Workshop den Umstand, dass der Lüfter bei Keshe's Aufbau läuft, und bei ihrem nicht, Keshe's grösserer Erfahrung zu.
Zu meiner Belustigung habe ich mir noch ein anderes Video angesehen:

GANS capture - set 2 - day 2 - GANS magneticaly structured
Externer Inhalt
Durch das Abspielen werden Daten an Youtube übermittelt und ggf. Cookies gesetzt.
Durch das Abspielen werden Daten an Youtube übermittelt und ggf. Cookies gesetzt.
Brüller ("the Plasma is created the same way")! Da ist der Meister ja auch selbst am Erklären. Jemand ne Idee, wie das Muster am Boden der Wanne zustande kommt. Vll. Plasma-Energy-Dendriten?
Keshe Foundation - Betrug und kein Ende in Sicht?
25.03.2014 um 04:11@Konfuse: Hmmm ... ich seh' da nur trübe Brühe. Die Frage ist, worum es sich bei der Trübung handelt. Die Brühe wird anscheinend in diesem Video eingesammelt:

Sie scheint also aus den Kupfer/Salzwasser/Kupfer(II)oxid-Zellen zu stammen. Keshe macht ein paar Aussagen dazu: Es werden in verschiedenen Zellen Salze verschiedener Herkunft verwendet. Bei bestimmten Salzarten bildet sich eine Trübung, bei anderen nicht. Im letzten Workshop erwähnte er, dass sich die Trübung nur bildet, wenn der Stromkreis geschlossen ist. Die entstehenden "Nanomaterialien" (die die Trübung verursachen) sind nach Isolierung bei diesem Aufbau grün oder blau. Vermutlich meint er damit sein "festes Methan". Dieses "feste Methan" sieht, wie schon früher festgestellt, verschiedenen Kupferverbindungen verdächtig ähnlich. Ziemlich naheliegend wäre bei diesem Experiment Kupfer(II)chlorid (in der stabilen Dihydrat-Form):

(Quelle: http://woelen.homescience.net/science/chem/compounds/cupric_chloride.html )
Hypothese: Durch die Verwendung unterschiedlicher Salzarten haben die Zellen unterschiedliche Innenwiderstände. In den Zellen mit höheren Innenwiderständen kommt es zu einer Elektrolyse. Dadurch kommt es der Kupferelektrode (Anode) zur Bildung von Kupfer(II)chlorid. Ich bin aber noch nicht sicher, ob das wirklich so passt.
In diesem Zusammenhang ist auch folgende Überlegung interessant: Keshe spricht im wesentlichen von zwei "festen Gasen", die er angeblich entdeckt hat: einmal das oben erwähnte "feste Methan" und zum anderen "festes CO2". Letzteres hat nach seiner Beschreibung eine gelartige Konsistenz.
Es wäre nun -- wie bereits erwähnt -- naheliegend, dass die silberfarbenen Elektroden in der anderen Variante des Experiments aus Zink bestehen. Sowohl Keshe's Bild seines "festen CO2" als auch die "gelartige Konsistenz" passen ganz hervorragend zu dem stark hygroskopischen Zinkchlorid:

Falls das elektrochemisch tatsächlich passt, wäre das Mysterium von Keshe's "festen Gasen" damit gelöst. :)

GANS capture - set 2 - day 2 - already started
Externer Inhalt
Durch das Abspielen werden Daten an Youtube übermittelt und ggf. Cookies gesetzt.
Durch das Abspielen werden Daten an Youtube übermittelt und ggf. Cookies gesetzt.
Sie scheint also aus den Kupfer/Salzwasser/Kupfer(II)oxid-Zellen zu stammen. Keshe macht ein paar Aussagen dazu: Es werden in verschiedenen Zellen Salze verschiedener Herkunft verwendet. Bei bestimmten Salzarten bildet sich eine Trübung, bei anderen nicht. Im letzten Workshop erwähnte er, dass sich die Trübung nur bildet, wenn der Stromkreis geschlossen ist. Die entstehenden "Nanomaterialien" (die die Trübung verursachen) sind nach Isolierung bei diesem Aufbau grün oder blau. Vermutlich meint er damit sein "festes Methan". Dieses "feste Methan" sieht, wie schon früher festgestellt, verschiedenen Kupferverbindungen verdächtig ähnlich. Ziemlich naheliegend wäre bei diesem Experiment Kupfer(II)chlorid (in der stabilen Dihydrat-Form):

(Quelle: http://woelen.homescience.net/science/chem/compounds/cupric_chloride.html )
Hypothese: Durch die Verwendung unterschiedlicher Salzarten haben die Zellen unterschiedliche Innenwiderstände. In den Zellen mit höheren Innenwiderständen kommt es zu einer Elektrolyse. Dadurch kommt es der Kupferelektrode (Anode) zur Bildung von Kupfer(II)chlorid. Ich bin aber noch nicht sicher, ob das wirklich so passt.
In diesem Zusammenhang ist auch folgende Überlegung interessant: Keshe spricht im wesentlichen von zwei "festen Gasen", die er angeblich entdeckt hat: einmal das oben erwähnte "feste Methan" und zum anderen "festes CO2". Letzteres hat nach seiner Beschreibung eine gelartige Konsistenz.
Es wäre nun -- wie bereits erwähnt -- naheliegend, dass die silberfarbenen Elektroden in der anderen Variante des Experiments aus Zink bestehen. Sowohl Keshe's Bild seines "festen CO2" als auch die "gelartige Konsistenz" passen ganz hervorragend zu dem stark hygroskopischen Zinkchlorid:

Falls das elektrochemisch tatsächlich passt, wäre das Mysterium von Keshe's "festen Gasen" damit gelöst. :)
Keshe Foundation - Betrug und kein Ende in Sicht?
25.03.2014 um 12:21Es sieht so aus, als müsste ich meine Theorie noch ein bisschen modifizieren. Der tschechische Knowledge Seeker Marek Istvanek hat bei YouTube einen tschechischen Workshop hochgeladen, in dem noch etwas mehr von den Vorgängen in den Zellen zu sehen ist, als in den bisherigen Videos.
Anscheinend bilden sich (ab ca. 01:09:00 im Video zu sehen) zum einen türkise Niederschläge im Bereich der Kupferelektrode (nur schwach zu sehen), aber auch türkise Ablagerungen an der Kupfer(II)oxid-Elektrode:

Erheblich deutlicher sieht man die Ablagerungen dann hier:

Meine Vermutung ist, dass der an der Kupfer(II)oxid-Elektrode (Kathode) entstehende Wasserstoff mit der Kupfer(II)oxid zu Kupfer und Wasser reagiert, und sich das Kupfer dann mit den neben dem Wasserstoff gebildeten Hydroxid-Ionen (OH) zu Kupfer(II)hydroxid verbindet. Kupfer(II)hydroxid ähnelt farblich dem oben abgebildeten Kupfer(II)chlorid (in Dihydrat-Form), und passt sehr gut zu dem Bild aus dem tschechischen Workshop:

Anscheinend bilden sich (ab ca. 01:09:00 im Video zu sehen) zum einen türkise Niederschläge im Bereich der Kupferelektrode (nur schwach zu sehen), aber auch türkise Ablagerungen an der Kupfer(II)oxid-Elektrode:

Erheblich deutlicher sieht man die Ablagerungen dann hier:

Meine Vermutung ist, dass der an der Kupfer(II)oxid-Elektrode (Kathode) entstehende Wasserstoff mit der Kupfer(II)oxid zu Kupfer und Wasser reagiert, und sich das Kupfer dann mit den neben dem Wasserstoff gebildeten Hydroxid-Ionen (OH) zu Kupfer(II)hydroxid verbindet. Kupfer(II)hydroxid ähnelt farblich dem oben abgebildeten Kupfer(II)chlorid (in Dihydrat-Form), und passt sehr gut zu dem Bild aus dem tschechischen Workshop:

Keshe Foundation - Betrug und kein Ende in Sicht?
25.03.2014 um 23:54Naja, bei den Wissenschuftlern muss man halt ganz genau hinsehen, damit man einen Effekt sieht. Ich habe mal ein Bild rauskopiert und den Kontrast erhöht. Viel ist nicht zu sehen, aber da ist schon ein Muster:uatu schrieb:Hmmm ... ich seh' da nur trübe Brühe.

Ist natürlich immer Spekulatius, weil man nie genau weiß, was die Brüder und Schwestern da verheimlichen. Aber ich gehe mit Dir in Deiner Annahme. Da ja etwas eintrübt bzw. etwas ausfällt, muss es sich um einen schlecht löslichen Stoff handeln. CuCl2 halte ich für unwahrscheinlich, eher ein Hydroxyd (ggf. auch Chloro-Misch-Komplexe, gibt viele Möglichkeiten, sind aber meist schwer löslich).uatu schrieb:Die Frage ist, worum es sich bei der Trübung handelt.
Es wäre nun -- wie bereits erwähnt -- naheliegend, dass die silberfarbenen Elektroden in der anderen Variante des Experiments aus Zink bestehen. Sowohl Keshe's Bild seines "festen CO2" als auch die "gelartige Konsistenz" passen ganz hervorragend zu dem stark hygroskopischen Zinkchlorid:Könnte sehr gut auch Al sein, das bildet sehr voluminöses Al(OH)3 bei (anodischer) Oxidation. Ist aber auch nur eine Vermutung.
Noch ein paar allgemeine Bemerkungen zu den Experimenten. Eigentlich ist das ganze Humbug, es soll ja ein kontinuierlicher Stromfluss erzeugt werden. Echte Batterien sind das aber nicht, da diese immer aus 2 Halbzellen bestehen. Dazu müsste jeweils eine Elektrode in eine Salzlösung gleichen Typs tauchen, also bei Cu etwa in eine Cu+ oder Cu2+ Lösung. Soweit meine Kenntnisse noch reichen, müsste es in dem Fall eine Cu(1+)-Lösung sein, damit eine kontinuierliche Reaktion stattfinden kann.
Trotzdem ist ja beim Meister zu sehen, dass der Lüfter kurz läuft, aber nicht dauerhaft und nur, wenn er wieder eine Zeit lang wartet. Meine Erklärung ist, dass sich nur ein diffusives Potential bildet, das schnell entladen ist. Will mich jetzt nicht zu weit aus dem Fenster lehnen, aber hat wahrscheinlich was damit zu tun:
Wikipedia: Helmholtz-Doppelschicht
Keshe Foundation - Betrug und kein Ende in Sicht?
26.03.2014 um 01:49@Konfuse:
Es kann gut sein, dass es sich bei der Trübung um irgendeinen Mischkomplex handelt, insbesondere auch weil die Keshies nach eigenen Angaben kein reines NaCl, sondern Meersalz u.ä. verwenden. Ein Chlorid als wesentliche Komponente halte ich u.a. für naheliegend, weil Keshe's "festes CO2" wirklich in jeder Hinsicht (Bilder, Beschreibung, etc.) ganz hervorragend zu Zinkchlorid passt. Lt. Keshe kann sich sein "festes CO2" verflüssigen -- genau das gilt wegen der sehr starken Hygroskopie auch für Zinkchlorid. Um es ganz eindeutig nachvollziehen zu können, müsste man es wohl ausprobieren -- dafür mangelt es mir allerdings an der Motivation.
Es kann gut sein, dass es sich bei der Trübung um irgendeinen Mischkomplex handelt, insbesondere auch weil die Keshies nach eigenen Angaben kein reines NaCl, sondern Meersalz u.ä. verwenden. Ein Chlorid als wesentliche Komponente halte ich u.a. für naheliegend, weil Keshe's "festes CO2" wirklich in jeder Hinsicht (Bilder, Beschreibung, etc.) ganz hervorragend zu Zinkchlorid passt. Lt. Keshe kann sich sein "festes CO2" verflüssigen -- genau das gilt wegen der sehr starken Hygroskopie auch für Zinkchlorid. Um es ganz eindeutig nachvollziehen zu können, müsste man es wohl ausprobieren -- dafür mangelt es mir allerdings an der Motivation.
Hatte ich zunächst auch gedacht, aber an verschiedenen Stellen sind Drähte angelötet. Es gibt zwar Tricks, um Aluminium zu löten, aber so ganz einfach ist das nicht.Konfuse schrieb:Könnte sehr gut auch Al sein ...
Es gibt durchaus auch (früher im Alltag eingesetzte) Batterien, die mit nur einer gemeinsamen Zelle arbeiten, z.B. das Lalande-Element. Auch eine Zitronenbatterie (die Keshe's Design vielleicht am nächsten kommt) hat nur eine Zelle.Konfuse schrieb:Echte Batterien sind das aber nicht, da diese immer aus 2 Halbzellen bestehen.
Keshe Foundation - Betrug und kein Ende in Sicht?
26.03.2014 um 01:55Falls jemand ein bisschen in Keshe's "USB-Stick"-Material stöbern möchte, ohne sich gleich die ganzen 1,6GB runterzuladen, gibt's das Ganze jetzt hier auch entpackt: http://open-source-energy.org/files/KF_org_data/ (Archiv-Version vom 22.04.2014)
Keshe Foundation - Betrug und kein Ende in Sicht?
26.03.2014 um 02:59Um ein paar naheliegenden Fragen zu Keshe's "USB-Stick"-Material zuvorzukommen: 1. Ja, das ist (zumindest gemäss grober Überprüfung) alles. 2. Nein, es gibt keine besonders interessante Stelle, die sich anzusehen lohnt. Das ist alles ungefähr gleich sinnlos. 3. Nein, ich weiss auch nicht, was sich Keshe dabei gedacht hat.
Keshe Foundation - Betrug und kein Ende in Sicht?
26.03.2014 um 14:02Rückblende: Eines der ungeklärten Rätsel im Zusammenhang mit Keshe ist, warum die Schröders nach ihrem erheblichen Engagement für Keshe (z.B. Ingrid Schröder's "Appell an Bundeskanzlerin Angela Merkel" (Archiv-Version vom 12.08.2016)) Mitte letzten Jahres plötzlich jede öffentliche Aktivität in Bezug auf Keshe eingestellt haben. Ingrid Schröder's http://forum.keshefoundation.org/search?searchJSON=%7B%22authorid%22%3A%5B%2227433%22%5D%7D sind von Ende Juni letzten Jahres, und lassen nichts ungewöhnliches erkennen. Danach hat weder sie noch ihr Mann sich meines Wissens nach je wieder öffentlich zum Thema Keshe geäussert.
Keshe Foundation - Betrug und kein Ende in Sicht?
26.03.2014 um 20:48@uatu
Hat jemand schon mal diese Schröders gesehen? Villeicht sind sie von Keshe fingierte Marionetten, die nur installiert wurden, um den Anschein von Unterstützern zu erwecken. Ihm würde ich alles zutrauen.
Andererseits könnten sie, falls sie echt sind, ja einfach ausgestiegen sein. Dann hätten sie aber bestimmt zum Abschluß noch was gepfeffertes gegen Keshe losgelassen.
Hat jemand schon mal diese Schröders gesehen? Villeicht sind sie von Keshe fingierte Marionetten, die nur installiert wurden, um den Anschein von Unterstützern zu erwecken. Ihm würde ich alles zutrauen.
Andererseits könnten sie, falls sie echt sind, ja einfach ausgestiegen sein. Dann hätten sie aber bestimmt zum Abschluß noch was gepfeffertes gegen Keshe losgelassen.
Keshe Foundation - Betrug und kein Ende in Sicht?
26.03.2014 um 22:37@Grymnir
Vielleicht ist das auch der Grund für das plötzliche Ende ihrer postings.
Zu der Zeit wurden noch alle Posts vom großen Meister einzeln freigegeben. Leute die ihre Meinung gegen die Cashe-Richtung ändern haben da ganz schnell eine Sperre.
Das einzig Mysteriöse ist, dass falls sie ausgestiegen sind, sie sich nie auf facebook, hier, oder sonstwo zu Wort gemeldet haben.
Wenn ich von Cashe gefoppt worden wäre, hätte die geneigte Leserschaft eine volle Breitseite über das halbe Netz beobachten können.
Vielleicht sind sie aber auch nur mit dem ersten Spaceship Prototypen eine Testrunde zur dunklen Seite des Mondes geflogen ;-)
Vielleicht ist das auch der Grund für das plötzliche Ende ihrer postings.
Zu der Zeit wurden noch alle Posts vom großen Meister einzeln freigegeben. Leute die ihre Meinung gegen die Cashe-Richtung ändern haben da ganz schnell eine Sperre.
Das einzig Mysteriöse ist, dass falls sie ausgestiegen sind, sie sich nie auf facebook, hier, oder sonstwo zu Wort gemeldet haben.
Wenn ich von Cashe gefoppt worden wäre, hätte die geneigte Leserschaft eine volle Breitseite über das halbe Netz beobachten können.
Vielleicht sind sie aber auch nur mit dem ersten Spaceship Prototypen eine Testrunde zur dunklen Seite des Mondes geflogen ;-)
Keshe Foundation - Betrug und kein Ende in Sicht?
26.03.2014 um 23:44@Grymnir: Die Schröders sind schon echt. Die waren u.a. bei verschiedenen Kongressen anwesend, wo das Thema Keshe behandelt wurde, und haben auch einige Präsenz-Seminare dazu veranstaltet (mangels Publikumsinteresse allerdings nicht viele). Hier kannst Du sie in Farbe sehen (rechts im Bild; der ganze Artikel ist von Frau Schröder): NET-Journal Januar/Februar 2013 (pdf). Frau Schröder hat auch eine Webseite. Das Seltsame an der Geschichte ist eben, dass es -- soweit mir bekannt -- keinerlei Stellungnahme o.ä. gab, warum die Schröders sich schlagartig und gänzlich von dem Thema zurückgezogen haben.
Keshe Foundation - Betrug und kein Ende in Sicht?
27.03.2014 um 04:30In einem bulgarischen Keshe-Forum, in dem ich seit Längerem mitlese, ist ein Teilnehmer, der dort öfters kritische Beiträge schreibt, bezüglich der aktuellen Experimente der Knowledge Seeker unabhängig zu ähnlichen Schlussfolgerungen gelangt, wie ich sie hier in den letzten Tagen beschrieben habe. Der Beitrag ist so interessant, dass ich ihn auszugsweise übersetzt habe:
Ich habe erwähnt, dass ich mich als Student intensiv mit elektrochemischen Experimenten beschäftigt habe. Wesentliche Elemente dabei waren Kupfer und Eisen, weniger Blei und Mangan (einmal aus dem Reduktionsgemisch einer Batterie), Chrom, Nickel, Zink. Was wir in dem Video sehen, ist die Konstruktion einer sehr ineffizienten galvanischen Zelle mit Kupferelektroden -- Kupfer + Kupferoxid. Ich werde nicht die Bezeichnung "Nanomaterial" verwenden, denn Nano-Eigenschaften haben nichts mit dem zu tun, was in dem unten beschriebenen Prozess geschieht, und die Entstehung von Kupferoxid ist ein klassischer oxidativer Korrosionsprozess, wie in allen Videos der Entstehung zu sehen ist. [...]Über den entscheidenden Punkt, die Bildung irgendwelcher Kupferchlorid/Kupferhydroxid-Verbindungen besteht also Einigkeit. Nicht einverstanden bin ich damit, dass das unterschiedliche Standardpotential von Kupfer und Kupferoxid die hauptsächliche Ursache der Spannung zwischen den Elektroden ist. Der Unterschied ist nämlich mit -0,34V für Kupfer und -0,36V für Kupferoxid (Tabelle -- ich habe nur den Wert für Kupfer(I)oxid gefunden, der von Kupfer(II)oxid dürfte aber ähnlich sein) zu gering, um sich nennenswert auszuwirken. Es ist erst der photovoltaische Effekt von Kupferoxid, der den allergrössten Teil der entstehenden Spannung erzeugt. Ausserdem vermute ich nach wie vor, dass die unterschiedlichen Innenwiderstände der Zellen ebenfalls eine Rolle spielen.
Reines Kupfer und und mit Kupferoxid beschichtetes Kupfer haben unterschiedliche elektrochemische Potentiale in Bezug auf Wasserstoff, so dass sie in einer wässrigen Elektrolytlösung unterschiedlich polarisiert werden und zwischen ihnen eine Spannung entsteht. Als Resultat tritt eine schwache Reaktion zwischen dem Natriumchlorid (Salz, Elektrolyt) in der Lösung und dem Kupferoxid auf (interne Elektrolyse in einer galvanischen Zelle), was zur Bildung der Komplexverbindung CuCl.CuOH.(nH2O) führt, einfach gesagt Monokupfer-chlorid-hydroxid-hydrat. Eigenartig bei der elektrolytischen chemischen Oxidation von Kupfer ist, wie ich festgestellt habe (und wie ich später gelesen habe, von anderen im Detail untersucht wurde), die Bildung von monovalenten Kupfersalzen. In unserem Fall in dem Video ist die Reaktion ist sehr schwach und ineffizient, die Verbindung wird in kleinen Mengen hergestellt und bleibt als Kolloid in Lösung - fällt nicht aus, und wenn man versucht, sie zu filtern, passiert sie die meisten Filter. Das Video zeigt deutlich den Tyndall-Effekt, die spezifische Lichtstreuung in einem Kolloid durch eine Taschenlampe.
(gegencho am 21.03.2014 [Google Translate EN / Google Translate DE])
Keshe Foundation - Betrug und kein Ende in Sicht?
27.03.2014 um 07:36In Keshe's Fukushima-Video gibt es einige Abschnitte, die weitere Hinweise auf die Beschaffenheit seiner "festen Gase" (von ihm auch als "GANS" = GAs + Nano + Solid state bezeichnet). Hier zunächst eine Sammlung verschiedener "GANS"-Proben:
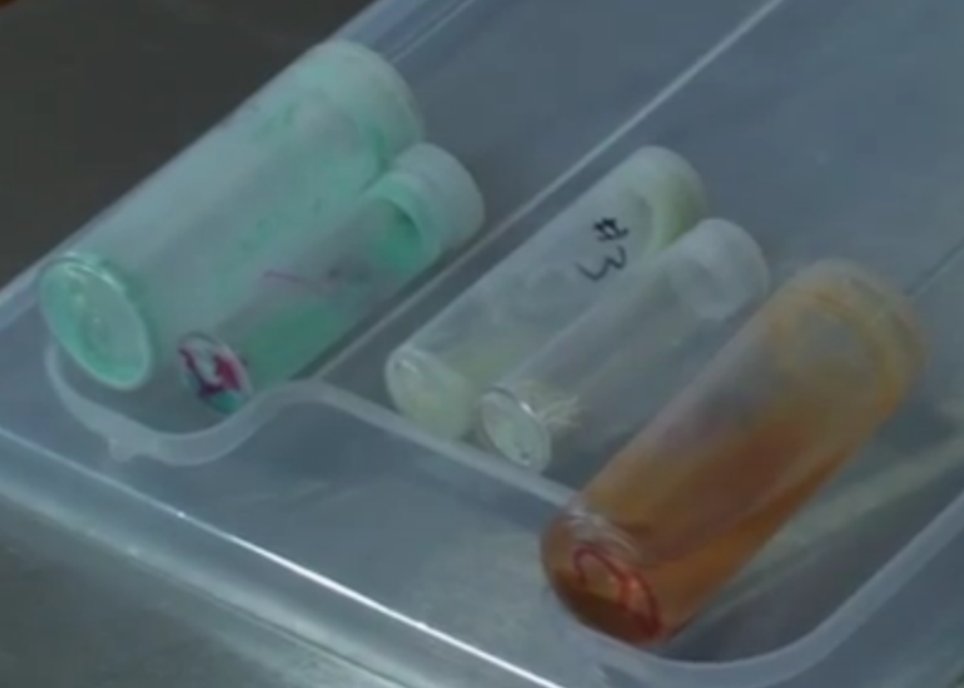
Neben den bekannteren türkisen und weissen Proben gibt es auch eine gelbbraune Probe. Dazu ist das Bild eines Zell-Kastens interessant, der anscheinend zur Erzeugung von Proben der letzteren Art dient:

Die Gitterelektroden sehen rostig aus, es handelt sich also sehr wahrscheinlich um Eisen. Die Komplementärelektroden haben einen grünlichen Belag, es handelt sich also sehr wahrscheinlich um Kupfer (vermutlich mit Keshe's üblicher Oxidschicht). Die Farbe der Ablagerungen in den Zellen passt gut zu meiner Chlorid-Theorie, sie ähnelt sehr der Farbe von Eisen(III)chlorid (in Hexahydrat-Form):

Das folgende Bild zweier Zell-Kästen könnte meine Theorie der unterschiedlichen Innenwiderstände der Zellen unterstützen:

Man sieht zum einen, dass der rechte Zell-Kasten erheblich stärkere Ablagerungen als der linke aufweist, und zum anderen, dass auch in den Kästen selbst die Zellen unterschiedlich starke Ablagerungen aufweisen. Insbesondere falls die beiden Kästen -- was naheliegend wäre -- zusammen eingesetzt wurden, würde das gut dazu passen, dass ein Teil der Zellen (die mit schwachen Ablagerungen) im Batterie-Modus arbeiteten, während die anderen Zellen (die mit starken Ablagerungen) im Elektrolyse-Modus arbeiteten.

Neben den bekannteren türkisen und weissen Proben gibt es auch eine gelbbraune Probe. Dazu ist das Bild eines Zell-Kastens interessant, der anscheinend zur Erzeugung von Proben der letzteren Art dient:

Die Gitterelektroden sehen rostig aus, es handelt sich also sehr wahrscheinlich um Eisen. Die Komplementärelektroden haben einen grünlichen Belag, es handelt sich also sehr wahrscheinlich um Kupfer (vermutlich mit Keshe's üblicher Oxidschicht). Die Farbe der Ablagerungen in den Zellen passt gut zu meiner Chlorid-Theorie, sie ähnelt sehr der Farbe von Eisen(III)chlorid (in Hexahydrat-Form):

Das folgende Bild zweier Zell-Kästen könnte meine Theorie der unterschiedlichen Innenwiderstände der Zellen unterstützen:

Man sieht zum einen, dass der rechte Zell-Kasten erheblich stärkere Ablagerungen als der linke aufweist, und zum anderen, dass auch in den Kästen selbst die Zellen unterschiedlich starke Ablagerungen aufweisen. Insbesondere falls die beiden Kästen -- was naheliegend wäre -- zusammen eingesetzt wurden, würde das gut dazu passen, dass ein Teil der Zellen (die mit schwachen Ablagerungen) im Batterie-Modus arbeiteten, während die anderen Zellen (die mit starken Ablagerungen) im Elektrolyse-Modus arbeiteten.
Keshe Foundation - Betrug und kein Ende in Sicht?
27.03.2014 um 10:39@Bertie
Ist bei den Opfern anderer Betrugsmaschen ja auch nicht anders.
Ich könnte mir vorstellen, daß es ihnen im Nachhinein einfach peinlich ist, jemals auf diesen hirnrissigen Müll hereingefallen zu sein, und sie einfach nur Gras darüber wachsen lassen wollen.Bertie schrieb:Das einzig Mysteriöse ist, dass falls sie ausgestiegen sind, sie sich nie auf facebook, hier, oder sonstwo zu Wort gemeldet haben..
Ist bei den Opfern anderer Betrugsmaschen ja auch nicht anders.
Keshe Foundation - Betrug und kein Ende in Sicht?
27.03.2014 um 19:02Keshe's Knowledge Seeker haben eine ganze Reihe neuer "GANS"-Videos veröffentlicht. Ich werde in Kürze näher darüber berichten. Es ist mir ein Rätsel, wieso die nicht merken, wie albern das ist, was sie da veranstalten.
Keshe Foundation - Betrug und kein Ende in Sicht?
27.03.2014 um 19:12@uatu
Also, ich schlage mal vor, die Halbreaktionen der Zelle zu formulieren, so wie es eigentlich nur ablaufen kann:
Kupferelektrode: Cu -> Cu1+ + e- (sorry, Hochzeichen gehen leider nicht)
Standardpotential: -0.520 V
Kupferoxidelektrode: Cu2+ + e- -> Cu1+
Standardpotential: +0.159
Der bulgarische Forist hat das genauso beschrieben. Die Standardpotentiale sind natürlich für die Verbindungen etwas anders, aber ein wenig Potentialdifferenz kommt da schon zustande.
An beiden Elektroden würde Cu1+ entstehen, was zwar leicht durch Sauerstoff oxidiert werden kann, aber auch schnell unlöslich Salze bildet. An der Kupferelektrode kann sich in einer Kochsalzlösung nur CuCl bilden. An der Kupferoxidelektrode kann es dazu kommen:
Und in Anwesenheit von Cl-Ionen natürlich auch alle möglichen Misch-Salz-Komplexe.
Wasserstoff kann dabei allerdings nicht gebildet werden, dazu bräuchte es ein unedleres Metall als Kupfer.
Leider habe ich meine damals hergestellten Elektroden schon entsorgt, sonst hätte ich die Zelle mal nachgebaut. Aber vll. mache ich auch mal demnächst neue, jetzt wo meine Experimentierlust wieder geweckt ist.
Also, ich schlage mal vor, die Halbreaktionen der Zelle zu formulieren, so wie es eigentlich nur ablaufen kann:
Kupferelektrode: Cu -> Cu1+ + e- (sorry, Hochzeichen gehen leider nicht)
Standardpotential: -0.520 V
Kupferoxidelektrode: Cu2+ + e- -> Cu1+
Standardpotential: +0.159
Der bulgarische Forist hat das genauso beschrieben. Die Standardpotentiale sind natürlich für die Verbindungen etwas anders, aber ein wenig Potentialdifferenz kommt da schon zustande.
An beiden Elektroden würde Cu1+ entstehen, was zwar leicht durch Sauerstoff oxidiert werden kann, aber auch schnell unlöslich Salze bildet. An der Kupferelektrode kann sich in einer Kochsalzlösung nur CuCl bilden. An der Kupferoxidelektrode kann es dazu kommen:
Reaktionsgleichung: 2 CuO + H2O + 2 e- -> 2 CuOHuatu schrieb:...was zur Bildung der Komplexverbindung CuCl.CuOH.(nH2O) führt, einfach gesagt Monokupfer-chlorid-hydroxid-hydrat.
Und in Anwesenheit von Cl-Ionen natürlich auch alle möglichen Misch-Salz-Komplexe.
Wasserstoff kann dabei allerdings nicht gebildet werden, dazu bräuchte es ein unedleres Metall als Kupfer.
Leider habe ich meine damals hergestellten Elektroden schon entsorgt, sonst hätte ich die Zelle mal nachgebaut. Aber vll. mache ich auch mal demnächst neue, jetzt wo meine Experimentierlust wieder geweckt ist.
Keshe Foundation - Betrug und kein Ende in Sicht?
27.03.2014 um 20:14@Konfuse:
CuO + H2O + 2 e[-] -> Cu[0] + 2 OH[-]
Was meinst Du dazu?
Das geht m.E. nicht auf (drei O links, zwei O rechts). In einem Lalande-Element passiert an einer CuO-Kathode mit einem KOH-Elektrolyt folgendes (ich gehe mal davon aus, dass das erwiesen ist):Konfuse schrieb:2 CuO + H2O + 2 e- -> 2 CuOH
CuO + H2O + 2 e[-] -> Cu[0] + 2 OH[-]
Was meinst Du dazu?
Keshe Foundation - Betrug und kein Ende in Sicht?
27.03.2014 um 20:33Hast recht, müsste eigentlich so aussehen:
CuO + H2O + e- -> CuOH + OH-
Hatte ich komischerweise auch erst formuliert. Interessant ist, das dabei OH- Ionen entstehen, das ganze wird also basisch (wie auch im Lalande-Element). Die Reaktionen (auch der Kupfer-Elektrode) können natürlich auch an der Kupferoxid/Kupfer-Elektrode alleine ablaufen. Deshalb meinte ich, dass eine echte Batterie eigentlich vernünftigerweise aus Halbzellen bestehen sollte.
Kann ja mal so was basteln, glücklicherweise habe ich auch pH-Meter, kann also mal testen.
CuO + H2O + e- -> CuOH + OH-
Hatte ich komischerweise auch erst formuliert. Interessant ist, das dabei OH- Ionen entstehen, das ganze wird also basisch (wie auch im Lalande-Element). Die Reaktionen (auch der Kupfer-Elektrode) können natürlich auch an der Kupferoxid/Kupfer-Elektrode alleine ablaufen. Deshalb meinte ich, dass eine echte Batterie eigentlich vernünftigerweise aus Halbzellen bestehen sollte.
Kann ja mal so was basteln, glücklicherweise habe ich auch pH-Meter, kann also mal testen.
Ähnliche Diskussionen